
 咨询热线:400-065-6886
咨询热线:400-065-6886

 咨询热线:400-065-6886
咨询热线:400-065-6886
从PubMed检索结果中来看,2020年6月10分以上主要有8篇文章介绍了m6A RNA甲基化领域的最新进展和综述总结:
1

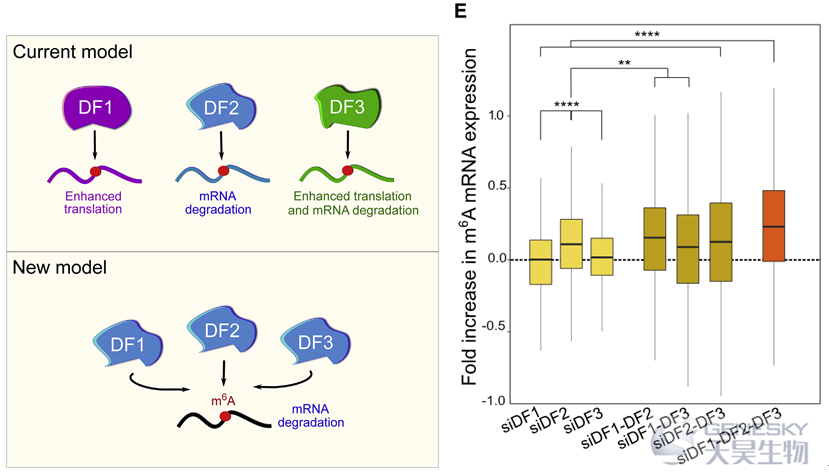
这项研究提出了一个完全不同的模型来解释m6A对mRNA的影响以及YTHDF1/2/3(DF)蛋白如何介导这些影响。与主流观点(不同的m6A位点结合不同的DF蛋白)不同的是,研究发现所有m6A位点以相似的方式结合了所有三种DF蛋白(上左图)。因此,所有的DF同源物都根据m6A位点的存在调节相同的mRNA。另外还发现,DF同源蛋白并不是翻译增强子,正如目前认为的DF1和DF3。相反,实验表明这三个DF的主要作用是促进mRNA的降解,在很大程度上是以冗余的方式(上左图)。DF敲除的冗余效应以前没有被检测到,是因为这些蛋白通常是单独敲除而没有进行同时敲除。只敲除一种蛋白质,其他同源蛋白就会有不同程度的补偿(上右图)。研究发现DF同源物具有相似的功能而不是不同的功能,这是由它们本质上相同的m6A结合属性、相似的相关结合蛋白集合以及它们共享的亚细胞定位所决定的。此外,这项研究表明,m6A对细胞分化的影响可以通过三种DF蛋白的联合作用来解释,而不是单个的DF蛋白。总的来说,这些研究揭示了一个新的m6A功能的统一模型,其中m6A主要通过三个冗余的DF蛋白的联合作用来影响相关mRNA的降解。
2

m6A在调节mRNA加工中起着重要作用。尽管该研究领域进展迅速,但对m6A修饰的遗传决定因素及其在常见疾病中的作用知之甚少。在本研究中,研究人员绘制了60个约鲁巴(YRI)淋巴母细胞样细胞系m6A peak的数量性状位点(QTLs)。结果发现m6A QTLs在很大程度上不依赖于表达和剪接QTLs,并且富集在RNA结合蛋白的结合位点,RNA结构改变的变体和转录特征。对m6A的QTLs和相关分子性状的联合分析表明,m6A的下游效应是异质性的、依赖于特定环境的。研究发现了介导m6A对翻译的影响的蛋白。通过整合全基因组关联研究的数据,发现了m6A QTLs对各种免疫和血液相关性状的遗传贡献度与剪接QTLs相当,大约是表达QTLs的一半。通过在转录组关联研究框架中利用m6A QTLs,可以确定这些性状的潜在的风险基因。
3

4

5


6


往期相关链接:
天昊生物

创新基因科技,成就科学梦想
微信扫一扫
关注该公众号
前往“发现”-“看一看”浏览“朋友在看”