
 咨询热线:400-065-6886
咨询热线:400-065-6886

 咨询热线:400-065-6886
咨询热线:400-065-6886
第一篇
01

第二篇
02

双链断裂(DSBs)是最有害的DNA损伤,如果不修复,可能会导致基因组不稳定或细胞死亡。这项研究报道了为应对DSBs,RNA甲基转移酶METTL3在S43位点被ATM介导的磷酸化激活。然后磷酸化的METTL3被定位到DNA损伤部位,在DNA损伤相关RNA中使得腺嘌呤N6位置发生甲基化修饰,进而招募m6A读蛋白YTHDC1进行保护。这样,METTL3-m6A-YTHDC1信号轴调控DSBs位点DNA-RNA杂合体的积累,然后招募RAD51和BRCA1进行同源重组(HR)介导的修复。而METTL3缺陷的细胞则表现出HR缺陷、未修复的DSBs积累和基因组不稳定。因此,METTL3缺失可显著提高癌细胞和小鼠异种移植模型对基于DNA损伤治疗的敏感性。这些发现揭示了METTL3和YTHDC1在HR介导的DSB修复中的作用,可能对癌症治疗有重要意义。
第三篇
03

T细胞METTL14缺失能够诱发小鼠自发性结肠炎。其特征是炎症细胞浸润增加,结肠重量/长度比增加,Th1和Th17细胞因子增加。结肠炎的发展是由于功能失调的调节性T (Treg)细胞,因为野生型Treg细胞过继转移减弱了结肠炎的表型。与野生型对照相比,METTL14缺陷Treg细胞降低了RORγt表达。METTL14缺陷导致naïve T细胞向诱导Treg细胞的诱导受损。抗生素治疗明显地减轻了结肠炎的发展。因此这项研究报道了基于干扰T细胞RNA甲基化的自发性结肠炎小鼠新的模型。结肠炎是T细胞介导的,并依赖于微生物组。这个模型可以为阐明致病途径,研究肠道微生物组的贡献和炎症性肠病治疗药物的临床前测试提供新的工具。
第四篇
04

表观遗传改变发生在许多生理和病理过程中。m6A修饰是真核mRNA中最常见的修饰。然而,m6A修饰在病理性血管生成中的作用仍不清楚。这项研究发现缺氧应激后,内皮细胞和小鼠视网膜中m6A修饰水平显著上调,这是由METTL3水平升高引起的。METTL3的沉默或过表达改变了体外内皮细胞的生存能力、增殖、迁移和管腔的形成。体内METTL3敲除降低了氧诱导视网膜病变模型的无血管区和病理性新生血管簇,抑制了碱烧伤诱导的角膜新生血管形成。机制上,METTL3通过m6A修饰靶基因(如LRP6和DVL1)来调控Wnt信号通路,发挥血管生成作用。METTL3增强了LRP6和DVL1的翻译,依赖于YTHDF-1。综上所述,本研究提示METTL3介导的m6A修饰是一种重要的缺氧应激反应机制。通过写蛋白METTL3靶向m6A是治疗血管生成性疾病的一项极有前景的策略。
第五篇
05

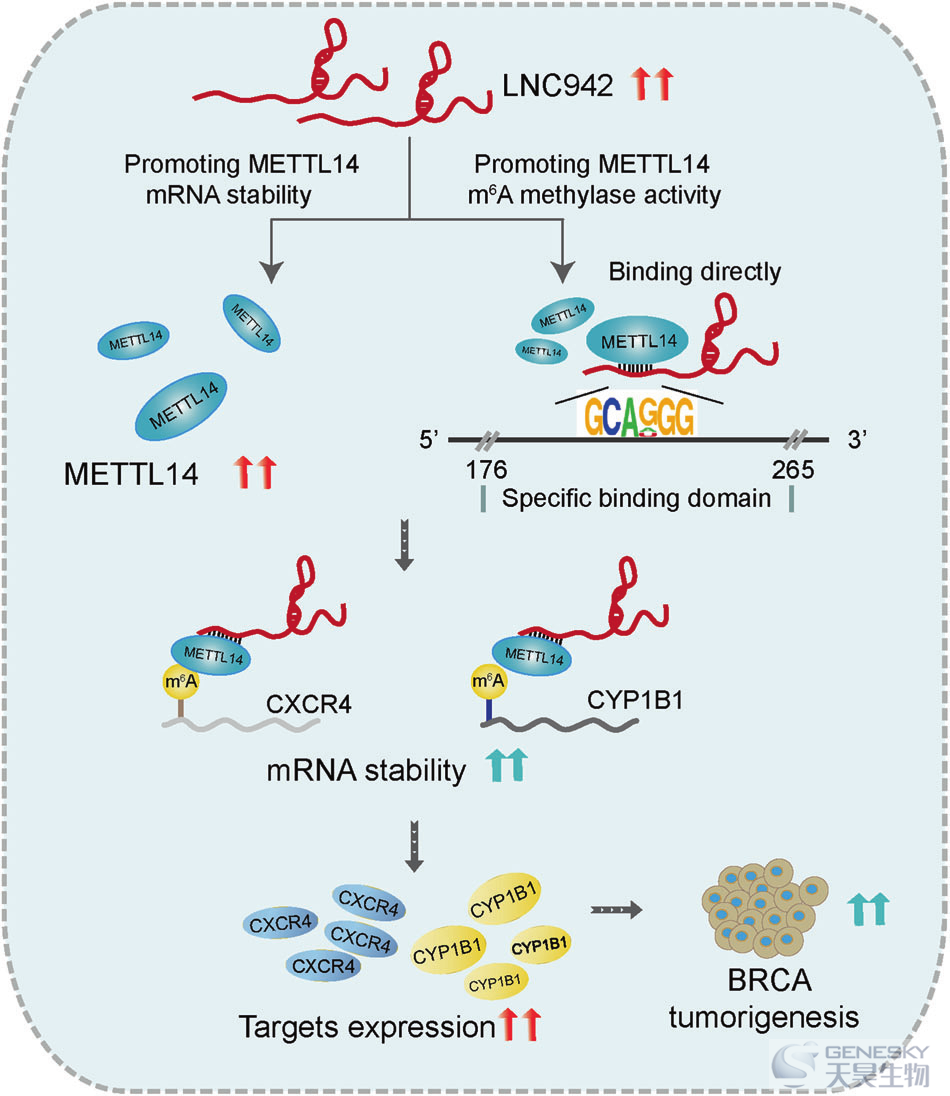
越来越多的证据支持lncRNAs在m6A表观遗传修饰水平作为肿瘤发生和发展的主调控因子。然而,乳腺癌(BRCA)的潜在调控机制仍不清楚。这项研究揭示了LINC00942 (LNC942)作为癌基因,在BRCA的起始和发展过程中,促进METTL14介导的m6A甲基化,调控其靶基因CXCR4和CYP1B1的表达和稳定性。具体来说,LNC942和METTL14在BRCA细胞和纳入的BRCA组(n = 150)中显著上调,同时伴有m6A修饰水平的上调。功能上,LNC942可诱发强的致癌作用,促进细胞增殖和菌落形成,抑制细胞凋亡,进而提高BRCA细胞中METTL14介导的m6A甲基化水平及其CXCR4、CYP1B1相关的mRNA稳定性和蛋白表达。机制上,LNC942通过具有特异性识别序列(+176—+265)直接招募METTL14蛋白,从而通过转录后m6A甲基化修饰在体内外稳定LNC942下游靶点CXCR4、CYP1B1的表达。因此,这项研究结果揭示了一个新的LNC942-METTL14-CXCR4/CYP1B1信号轴,为BRCA的防治提供了新的靶点和交互m6A表观遗传修饰机制。
第六篇
06

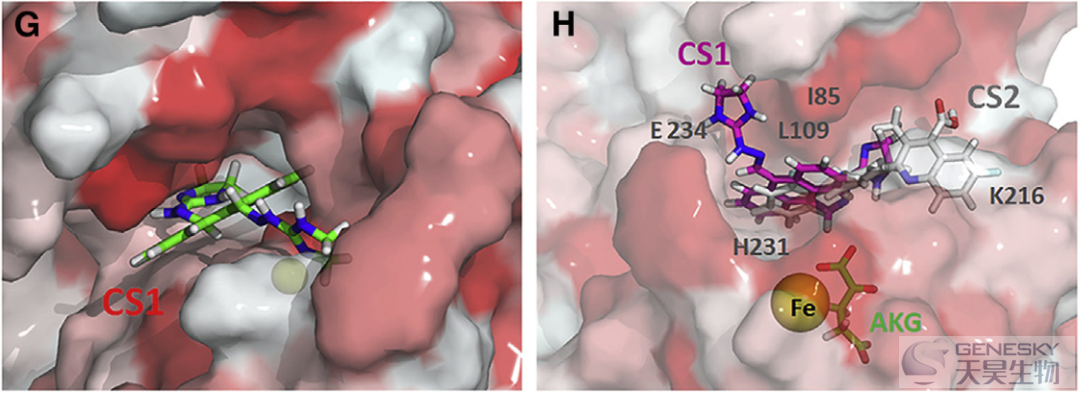
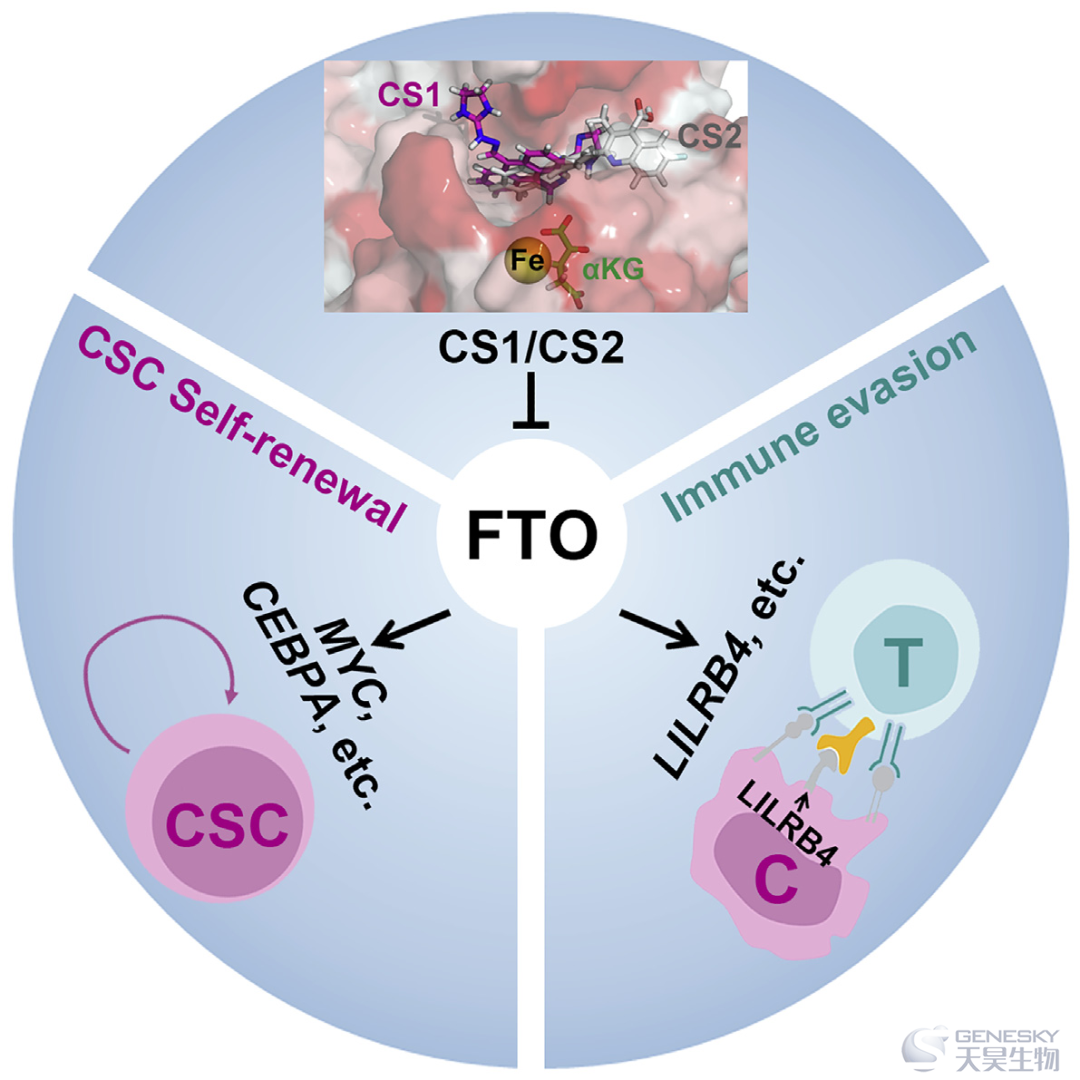
恶性胶质瘤是成人致死性的原发性脑瘤之一。如此糟糕的预后要求我们更好地理解这种疾病的癌症相关信号通路。这项研究阐明了在胶质瘤中调节增殖和肿瘤发生的一个MYC-miRNA-MXI1反馈回路。MYC通过miR-155和miR-23a簇抑制MXI1的表达,而MXI1则通过与MYC启动子结合抑制其表达。过表达miR-155和miR-23a簇促进U87胶质瘤细胞的肿瘤发生。此外,m6A RNA去甲基化酶FTO通过靶向MYC调节这一回路。甲氯灭酸乙酯(MA2)抑制FTO,增强化疗药物替莫唑胺(TMZ)抑制胶质瘤细胞增殖的作用,并负向调节回路。这些数据共同强调了胶质瘤的一个关键调节回路,并为临床治疗提供了潜在的靶点。
往期相关链接:


创新基因科技,成就科学梦想
微信扫一扫
关注该公众号
前往“发现”-“看一看”浏览“朋友在看”